长春应化所在超声触发纳米药物深层肿瘤渗透方面取得重要进展
中国科学院长春应用化学研究所在利用超声触发纳米药物电荷反转以增强实体瘤深层渗透的研究中取得重要进展。研究团队首次揭示了香豆素衍生的氨基甲酸酯键的超声响应裂解机制,并创新性地将该结构用于构建可超声遥控的电荷反转纳米递送系统。该系统在低强度超声作用下发生快速电荷翻转,激活高尔基体依赖性迭代转胞吞通路,最终实现了纳米药物在实体瘤中的深度穿透与高效低毒治疗(图1)。相关研究成果以“Ultrasound-Triggered Charge-Reversal Nanoparticles via Golgi-Dependent Iterative Transcytosis for Enhanced Deep Tumor Penetration”为题,发表于《ACS Nano》。
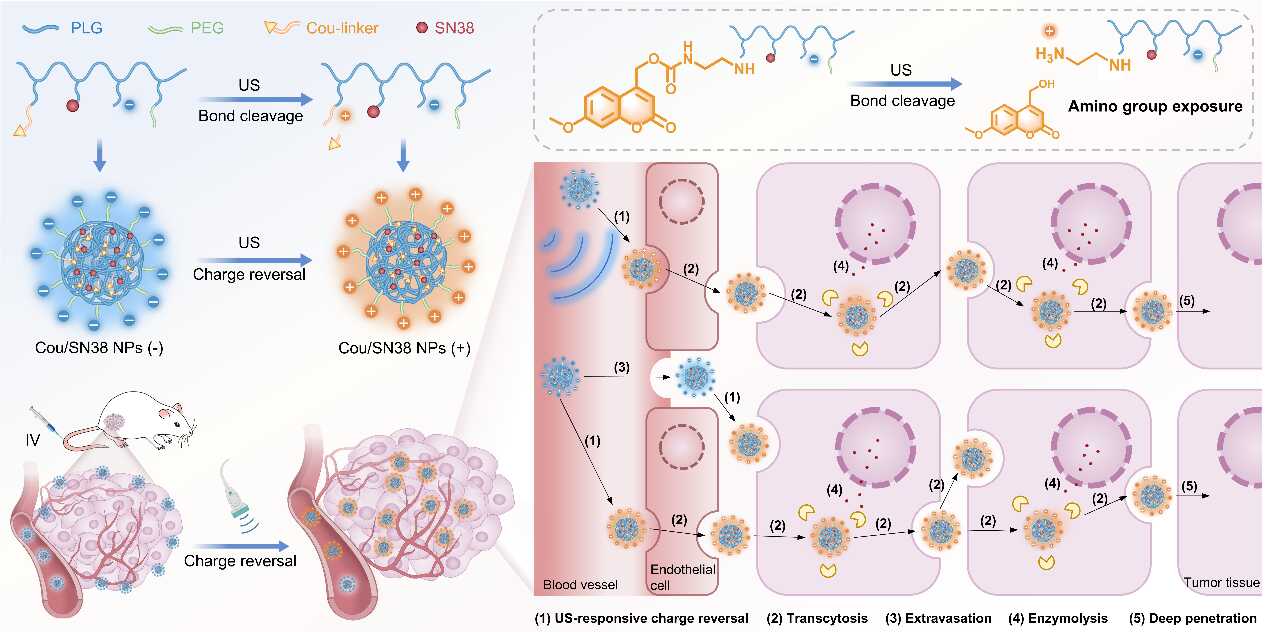
图1. 超声触发电荷反转纳米颗粒通过高尔基体依赖性迭代转胞吞作用实现深层肿瘤渗透的工作机制示意图
长期以来,实体瘤内致密的细胞外基质与高间质流体压力构成了纳米药物向肿瘤深部递送的核心屏障,导致药物难以在肿瘤核心区域达到有效治疗浓度。传统的肿瘤微环境(pH、酶)响应型电荷翻转策略常受限于肿瘤异质性及响应动力学缓慢,难以实现药物的均匀深层渗透;而光响应策略虽反应迅速,却受限于生物组织穿透深度不足的固有短板。因此,发展一种兼具深层穿透能力与快速时空可控性的药物递送新策略,成为该领域亟待解决的关键科学问题。
针对上述难题,陈学思院士、汤朝晖研究员团队基于超声的非侵入性、深部穿透及高时空分辨率特性,研发出新型超声响应化学单元——香豆素衍生的氨基甲酸酯键。理论计算与实验证实,在理疗级低强度超声(1.5 W/cm², 1 MHz, 50%占空比)作用下,该化学键可发生高效断裂并暴露出可质子化的伯氨基,从而实现表面电荷的快速转变(图2)。在此基础上,研究团队以聚谷氨酸(PLG)为骨架,构建了负载SN38的超声触发电荷反转纳米颗粒(Cou/SN38 NPs)。该纳米系统在生理环境中表面带负电,可维持长循环稳定性;经肿瘤部位超声辐照仅数分钟,即可实现表面电位由负到正的彻底翻转,展现出极高的时空可控性。值得注意的是,肿瘤微酸性环境可进一步加速该电荷翻转进程,赋予了该体系内在的肿瘤选择性(图3)。
更为重要的是,研究团队深入阐明了电荷反转所触发的细胞转运机制转变。研究发现,超声触发电荷反转后,纳米颗粒的细胞主要内吞途径从巨胞饮转变为小窝蛋白介导的内吞,且细胞内运输轨迹发生根本性改变,带正电的纳米颗粒更倾向于被转运至高尔基体而非溶酶体,成功激活了高尔基体依赖性的迭代转胞吞过程。该过程使纳米颗粒能被肿瘤细胞高效内化,经高尔基体包装后再次排出,并被邻近肿瘤细胞重复摄取,实现了药物在肿瘤组织中的接力传递。在针对4T1小鼠乳腺癌模型的系统性评价中,该策略展现了卓越的抗肿瘤效果。在活体动物水平,静脉注射Cou/SN38 NPs并结合肿瘤部位局部超声辐照后,药物在肿瘤深部的富集量显著增加,最终实现了高达93%的肿瘤生长抑制率,且未观察到明显的系统性毒副作用,部分小鼠的肿瘤实现了完全治愈(图4)。
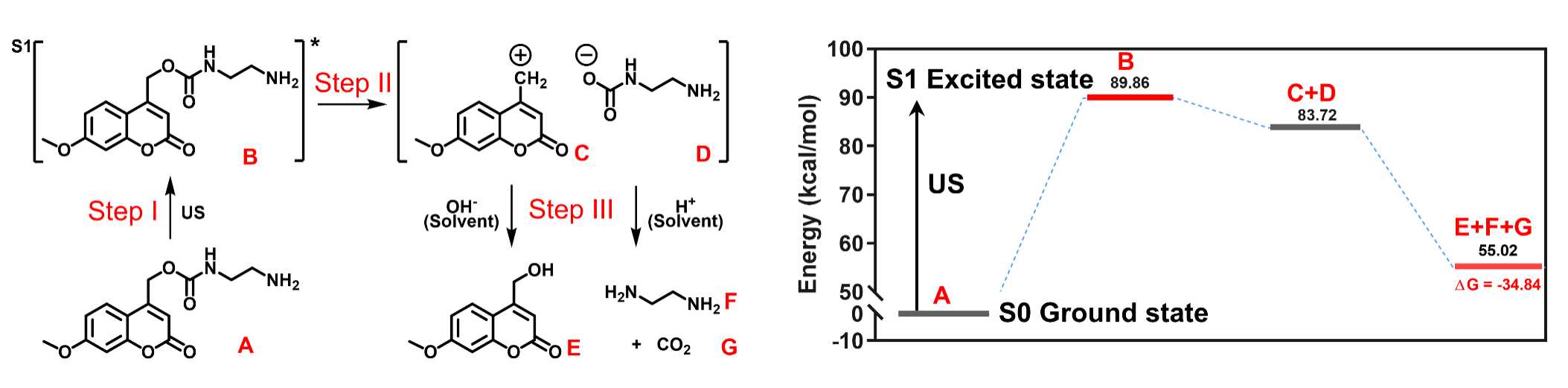
图2. 香豆素衍生的氨基甲酸酯键的超声裂解机制
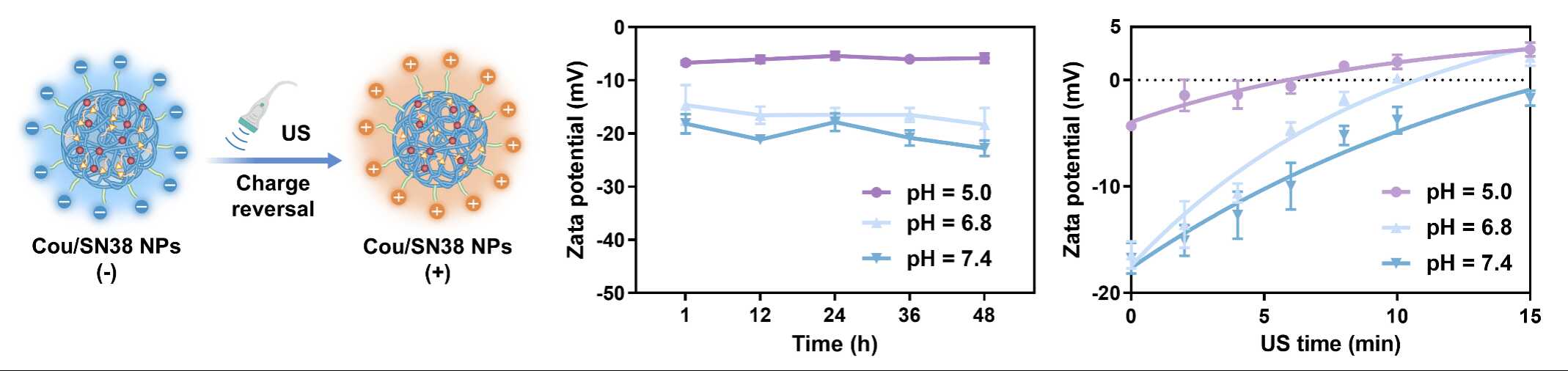
图3. 超声触发电荷反转纳米颗粒Cou/SN38 NPs的电荷精准调控
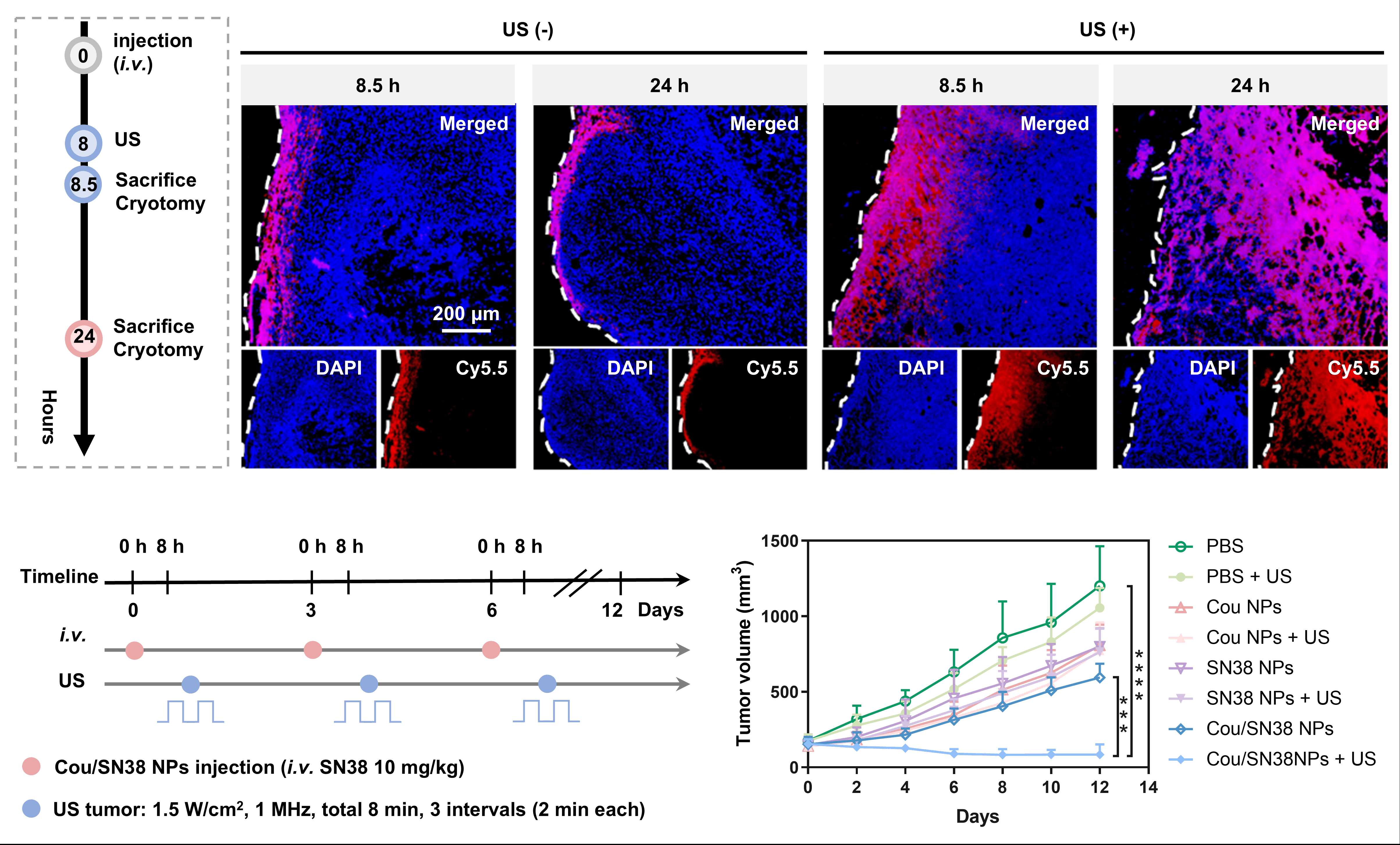
图4. 超声触发电荷反转纳米颗粒Cou/SN38 NPs在实体瘤中的深层渗透和显著抑瘤效果
该研究的创新之处在于将全新的超声响应化学反应用于纳米药物的电荷反转设计,相较于传统策略,兼具响应速度快、组织穿透能力强、时空可控性高的优势,为克服纳米药物的肿瘤渗透难题提供了全新思路,也彰显了超声响应化学在肿瘤精准治疗领域的广阔应用前景。
研究成果详见《ACS Nano》期刊:https://doi.org/10.1021/acsnano.5c14557



