长春应化所在高密度异核双原子纳米酶的构建及肿瘤代谢免疫调控领域取得重要进展
中国科学院长春应用化学研究所在高密度异核双原子纳米酶的构建及肿瘤代谢免疫调控领域取得重要进展。张洪杰院士和王樱蕙研究员研究团队成功开发出一种高密度异核 Fe/Co 双原子纳米酶平台,可通过诱导双硫死亡和铁死亡用于抗肿瘤免疫治疗,该纳米酶负载高密度 Fe/Co 双金属活性中心(Fe、Co 质量分数分别达10.35 wt%、11.32 wt%),具有优异的类核黄素酶和类过氧化物酶活性,可高效催化生物硫醇氧化,破坏肿瘤细胞氧化还原稳态。相关研究成果以“Charge-Tunable Dense Dual-Atom Nanozymes Reprogram Biothiol Metabolism Through Multi-Enzyme-Mimetic Catalysis to Synergistically Induce Ferroptosis and Disulfidptosis”为题,发表于国际权威化学期刊《Angewandte Chemie International Edition》。
生物硫醇在维持细胞氧化还原稳态、调控程序性细胞死亡途径及调节免疫反应中发挥关键作用。因此,对肿瘤细胞的生物硫醇代谢进行重编程,是增强抗肿瘤免疫的一种极具前景的策略。高密度异核双原子纳米酶具有不对称电子分布、原子级协同作用及超高活性位点密度等显著特征,近年来已成为克服传统单原子纳米酶固有局限性的有效手段,为高效调控生物硫醇代谢提供了新的机遇。
基于以上思路,研究团队设计并制备了一种天然多酚根皮苷修饰的高密度铁-钴双原子纳米酶平台(FeCo DDA/P)。具有优化电子结构的高密度铁-钴双原子催化位点,赋予FeCo DDA优异的类过氧化物酶(POD)、类L-半胱氨酸氧化酶(LCO)、类谷胱甘肽氧化酶(GSHOx)及类NADPH氧化酶(NOx)活性。FeCo DDA/P不仅可通过本征多酶活性高效产生活性氧、消耗谷胱甘肽并生成内源性过氧化氢以放大肿瘤细胞内的氧化应激,诱导免疫原性铁死亡;还可以阻断糖酵解过程并直接氧化L-半胱氨酸和打破NADP+/NADPH的氧化还原平衡,导致胱氨酸积累并启动双硫死亡。FeCo DDA/P诱导的级联增强的铁死亡和双硫死亡进一步刺激树突状细胞成熟,逆转免疫抑制性肿瘤微环境,从而增加T细胞浸润并激活全身性抗肿瘤免疫。综上,FeCo DDA/P可有效破坏氧化还原稳态、重编程生物硫醇代谢,进而触发双瘤死亡和铁死亡,实现高效肿瘤抑制与强效免疫激活的双重效果(图1)。
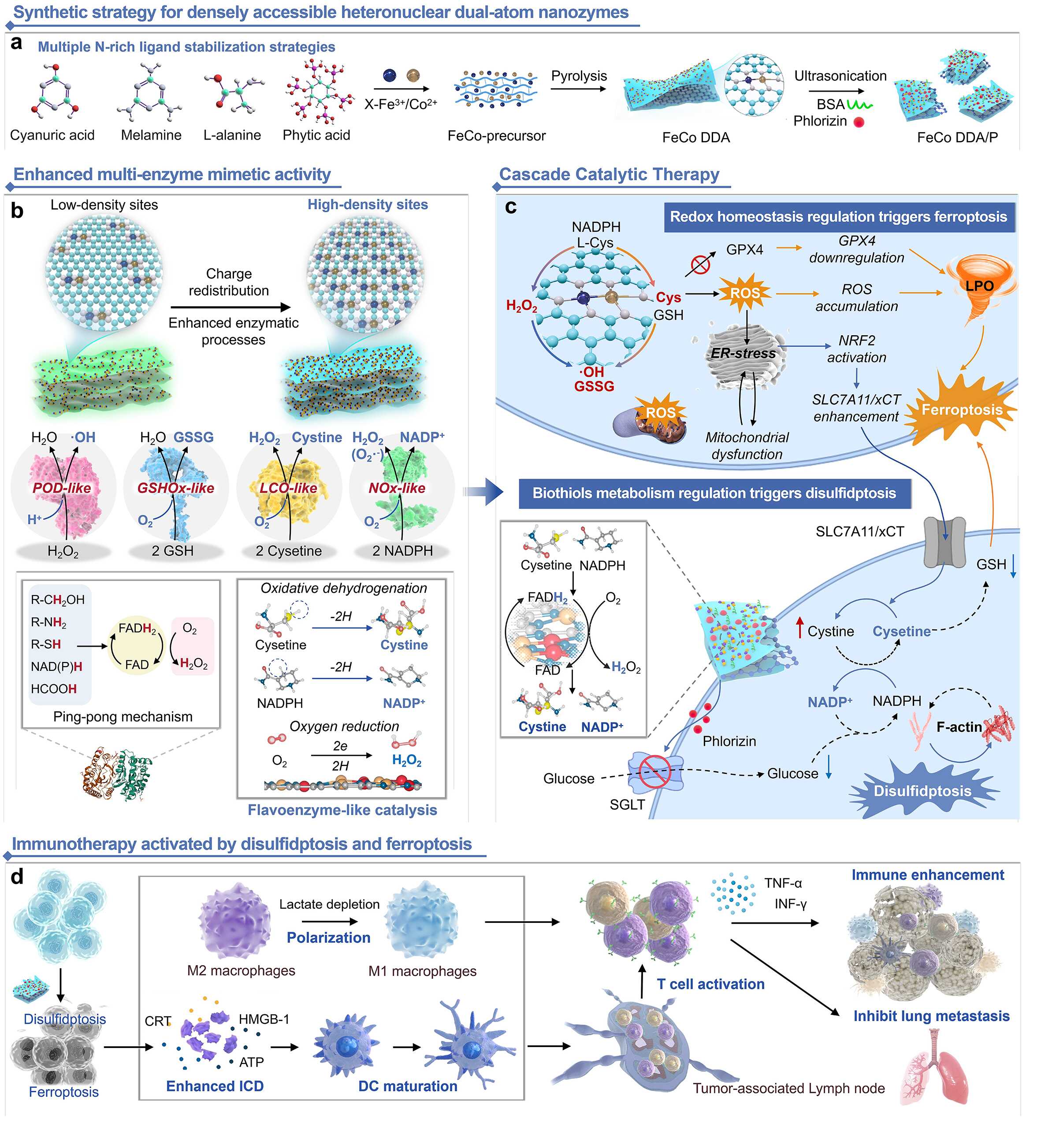
图1. FeCo DDA/P 的制备及其治疗机制示意图
本研究通过“原位缩聚与限域碳化”策略制备了负载高密度Fe/Co原子对的双原子纳米酶,不仅为多功能纳米酶的原子级设计提供了新策略,也为在肿瘤精准治疗中利用铁死亡与双硫死亡作为协同免疫调控机制构建了理论框架。
研究成果详见《Angewandte Chemie International Edition》期刊: https://doi.org/10.1002/anie.202524634



